Fiches pratiques
RetourRéférentiel multidisciplinaire de l’Amylose Cardiaque
Fiche MULTIDISCIPLINAIRE – Epidémiologie & Suspicion des Amyloses Cardiaques (AL et ATTR)
PARTIE 1 : MÉDECINE INTERNE
Rédigée par le Pr. Jacques POUCHOT
Les amyloses cardiaques sont de 2 types :
〉L’amylose AL, liée à des dépôts de chaînes légères d’immunoglobulines, majoritairement de type lambda (le plus souvent dans le contexte d’une gammapathie monoclonale de signification indéterminée [MGUS : Monoclonal Gammopathy of Unknown Significance] ou plus précisément dans ce cas de signification clinique [MGCS : Monoclonal Gammopathy of Clinical Significance] ou plus rarement d’un myélome multiple ou d’un lymphome).
〉Les amyloses à transthyrétine (TTR) dont il existe deux types selon que les dépôts sont constitués de TTR sauvage (TTRwt : wild type) ou mutée (TTRm : mutée).
〉Les autres types d’amylose (AA notamment) ne se compliquent qu’exceptionnellement d’une atteinte cardiaque.
Données épidémiologiques
〉L’amylose AL est rare. Il n’y a pas de données épidémiologiques françaises mais si l’on retient une incidence annuelle identique à celle des États-Unis (9 cas par million d’habitants), le nombre de nouveaux cas d’amylose AL en France serait d’environs de 500 par an en France. La maladie est un peu plus fréquente chez l’homme et l’âge moyen au diagnostic est de 65 ans. L’atteinte cardiaque isolée est rare, observée dans moins de 5 % des cas.
〉Les amyloses à TTRm sont de transmission autosomique dominante mais de pénétrance incomplète. De nombreuses mutations (>140) du gène de la transthyrétine (TTR) ont été rapportées et sont associées à des phénotypes à prédominance cardiaque, neurologique ou mixte. La prévalence des amyloses à TTRm en France n’est pas connue mais environ 8 % des patients de plus de 60 ans ayant une cardiopathie hypertrophique ont une mutation de TTR. L’âge des malades au diagnostic est de plus de 60 ans et parfois plus pour certaines mutations.
〉L’amylose à TTRwt est une maladie du sujet âgé, beaucoup plus fréquente que les amyloses à TTRm. On estime que 13 % à 18 % des patients ayant une insuffisance cardiaque à fraction d’éjection préservée ont une amylose à TTR, le plus souvent de type TTRwt. Par ailleurs, dans les études post-mortem, des dépôts cardiaques d’amylose à TTRwt sont trouvés chez environ 25 % des patients de plus de 80 ans.
Le diagnostic d’amylose cardiaque est encore trop souvent fait avec retard et certaines manifestations liées aux dépôts d’amylose pouvant précéder l’atteinte cardiaque de plusieurs années méritent donc d’être connues.
〉Syndrome du canal carpien. Il peut s’observer dans tous les types d’amylose mais plus souvent avec l’amylose à TTRwt. La suspicion d’amylose doit être plus grande devant un syndrome du canal carpien bilatéral chez un sujet de plus de 50 ou 60 ans et en l’absence de cause classique (rhumatisme inflammatoire, hypothyroïdie notamment). La fréquence des dépôts amyloïde varie entre 10 et 35% des cas et l’amylose est d’autant plus fréquente que le syndrome du canal carpien est bilatéral et que le sujet est plus âgé. Même si une amylose cardiaque est parfois dépistée au moment du diagnostic du syndrome du canal carpien, celui-ci précède le plus souvent la survenue d’une amylose cardiaque clinique, de 5 à 10 ans en moyenne pour les amyloses à TTR. L’évolution des amyloses AL est en règle générale plus rapide.
〉Canal lombaire rétréci. Chez des patients opérés pour un canal lombaire rétréci les prélèvements systématiques de fragments de ligaments jaunes montrent des dépôts amyloïdes à TTRwt le plus souvent chez 33 à 45% et ceux-ci sont plus fréquents en présence d’un antécédent de canal carpien opéré ou chez les sujets les plus âgés. Les symptômes du canal lombaire rétréci précèdent généralement de plusieurs années la survenue des premières manifestations de l’amylose cardiaque.
〉D’autres manifestations liées à l’amylose à TTR ont été rapportées : rupture du tendon du long biceps, surdité de perception, arthrose, maladie de Dupuytren. Ces manifestations sont toutefois très peu spécifiques. Il faut aussi savoir rechercher une amylose à TTR devant un rétrécissement aortique serré (présente chez 6 à 16% des malades). La présence d’une neuropathie périphérique axonale et longueur dépendante peut faire discuter une amylose à TTRm, parfois associée à une atteinte cardiaque.
〉Autres manifestations liées à l’amylose AL : ecchymoses classiquement périorbitaires, purpura, atteintes articulaires, macroglossie, pseudo-hypertrophie musculaire des épaules, atteinte rénale (néphropathie glomérulaire).
Conclusions
Un diagnostic d’amylose à TTR sauvage ou mutée ou d’amylose AL peut être suspecté devant le tableau clinique suivant :
〉un(e) patient(e) généralement de plus de 60-65 ans
〉ayant un antécédent de syndrome du canal carpien opéré ou non et le plus souvent bilatéral
〉ou un antécédent de canal lombaire rétréci opéré
Vous pouvez demander une consultation en Médecine interne selon les modalités suivantes :
|
PARTIE 2 : GÉRIATRIE
Rédigée par le Dr Julien LE GUEN.
Une insuffisance cardiaque du sujet âgé sans étiologie apparente, à fortiori lorsque la fraction d’éjection est préservée justifie une exploration diagnostique et doit faire évoquer une amylose.
Devant un tableau clinique évocateur d’amylose chez un sujet de plus de 75 ans, la consultation spécialisée peut être orientée vers l’équipe de Gériatrie de l’HEGP.
Vous pouvez adresser la demande de consultation au secrétariat selon les modalités suivantes :
|
Préciser :
〉« Demande de consultation amylose »
〉Le contexte clinique motivant la demande
〉Le degré d’urgence de la consultation
〉Les coordonnées et informations personnelles essentielles du/de la patient(e)
〉Joindre un courrier avec antécédents médicaux et traitements en cours du/de la patient(e) (ou s’assurer a minima que ces informations seront disponibles au moment de la consultation en gériatrie)
La consultation de gériatrie permet une évaluation « globale et standardisée » comprenant notamment :
- l’autonomie et l’environnement social ;
- les éventuelles difficultés cognitives et leur retentissement ;
- les besoins d’interventions à domicile ;
- les comorbidités et leur retentissement ;
- l’organisation médicamenteuse (observance, accès aux traitements, bilan de médication)
- les troubles de l’équilibre et les chutes,
- les troubles sensoriels.
Cette évaluation conduit à l’élaboration de recommandations, qui peuvent justifier un suivi et/ou des explorations complémentaires spécialisées.
PARTIE 3 : HÉMATOLOGIE
Rédigée par le Dr Luc DARNIGE
Arguments cliniques et biologiques du point de vue de l’hématologue (1)
〉Purpura périorbitaire
〉Macroglossie
〉Déficit en facteur X de la coagulation-syndrome hémorragique
〉MGUS atypique ou Myélome indolent
〉MGUS associé à un ratio CLL anormal et un NT-proBNP élevé et/ou une protéinurie
MGCS : Monoclonal Gammopathy of Clinical Significance (2)
- Amylose AL : 75% sont des AL à CLλ ; 25% sont des AL à CLκ ; <10% sont des AL issues d’IgM
- Randall : dépôt uniquement de CL, généralement κ
(1) Merlini G, et al. Systemic immunoglobulin light chain amyloidosis. Nat Rev Dis Primers. 2018 Oct 25;4(1):38.
(2) Fermand JP, et al. Monoclonal gammopathy of clinical significance: a novel concept with therapeutic implications. Blood. 2018 Oct 4;132(14):1478-1485.
Devant un bilan biologique évocateur, vous pouvez adresser votre patient à l’HEGP pour une exploration hématologique approfondie.
Pour cela, contactez
|
le Dr Luc DARNIGE par mail : luc.darnige@aphp.fr |
en fournissant les informations suivantes :
〉Le contexte clinique
〉Les examens récents : NFS, EPP, Ionogramme, Créatininémie, Calcémie
Préciser :
〉Lestraitementsencours(notammentanticoagulants)
〉Si antécédents de sternotomie et de radiothérapie du thorax
L’exploration biologique comprendra, selon le contexte :
- Electrophorèse des protéines sériques avec Immunofixation : B160
- Immunofixation des protéines urinaires (Protéinurie de Bence-Jones 24h) : B180
- Dosage pondéral des immunoglobulines sériques : B66
- Dosage des chaînes légères libres : BHN150x0,27 €
- Myélogramme : ponction aspiration de la moelle osseuse hématopoïétique (ce n’est pas une ponction lombaire) réalisée, au lit du patient, en sternal ou en crête iliaque, après anesthésie locale (xylocaïne) par un personnel entrainé. Le geste lui-même ne dure pas plus d’une minute et la douleur a été évaluée par les patients en EVA à 3,4 (échelle de 0 à 10). (1)
(1) Gendron N et al. Pain assessment and factors influencing pain during bone marrow aspiration: A prospective study. PLoS One. 2019 Aug 29;14(8):e0221534.
PARTIE 4 : NÉPHROLOGIE
Rédigée par le Pr Alexandre KARRAS
Atteintes rénales
〉Protéinurie et syndrome néphrotique : AL (1)
〉Insuffisance rénale chronique : ATTRwt/h, AL (1)
• Classiquement : Microalbuminurie (avant ou 3 à 5 ans après de diagnostic) > Néphropathie (2 ans après la microalbuminurie) > IRC (5 ans après la microalbuminurie) > Dialyse (10 ans après la microalbuminurie). (2)
Atteintes rénales dans l’ATTR
〉Jusqu’à 37 % des ATTRh (3)
〉15 % des ATTRwt / 20 % des ATTRh Val122Ile (4)
(1) Zhang KW, et al. Am J Med. 2021 May;134(5):587-595. (2) Lobato L, et al. Clin J Am Soc Nephrol. 2012 Aug;7(8):1337-46. (3) Ferraro PM, et al. Brain Sci. 2021 Jul 24;11(8):980. (4) Maurer MS, et al. J Am Coll Cardiol. 2016 Jul 12;68(2):161-72.
PARTIE 5 : GASTRO-ENTEROLOGIE
Rédigée par le Dr Sherine KHATER.
Présentation clinique
L’amylose est une maladie rare, caractérisée par un dépôt de substance amyloïde dans les tissus (cœur, système nerveux, rein), y compris les organes digestifs.
L’atteinte histologique du tube digestif existe chez presque tous les patients porteurs d’une amylose systémique, mais les manifestations cliniques surviennent dans 56 à 69 % des cas. Elles ont un impact important sur la qualité de vie des patients. Les présentations cliniques sont très variables et les symptômes sont peu spécifiques, pouvant souvent mimer un trouble fonctionnel de l’intestin, ce qui rend le diagnostic difficile. Les mécanismes physiopathologiques responsables de l’atteinte digestive sont multiples :
- l’atteinte du système nerveux autonome, responsable de troubles moteurs à tous les niveaux.
- les dépôts diffus dans la paroi digestive ainsi que les dépôts vasculaires.
- la colonisation bactérienne chronique du grêle
Les principales manifestations digestives sont les suivantes (tableau 1) : (1)
|
〉Œsophage : principalement dysphagie et reflux gastro- œsophagien. 〉Estomac : L’atteinte gastrique est surtout la conséquence de l’atteinte du système nerveux autonome et se traduit par un syndrome dyspeptique, des nausées et des vomissements en rapport avec une gastroparésie. L’aspect endoscopique est la plupart du temps normal ou peu modifié : il peut s’agir d’un aspect finement granuleux, polypoïde, érodé, voire ulcéré. 〉Intestin grêle : diarrhée sévère avec malabsorption et amaigrissement. Le mécanisme de cette diarrhée est complexe et multifactoriel (atteinte du système nerveux autonome, malabsorption, colonisation bactérienne chronique du grêle…). 〉Colon et rectum : troubles du transit (diarrhée, constipation ou alternance diarrhée et constipation) ou incontinence fécale. Les lésions endoscopiques ressemblent à celles qui ont été décrites au niveau du tractus digestif supérieur. La calprotectine fécale est le plus souvent élevée chez ces patients. |
Tableau 1 : Fréquence des symptômes gastro-intestinaux chez les patients ayant une amylose héréditaire liée à l’ATTR.
|
Diagnostic
Le diagnostic positif de l’amylose repose sur la mise en évidence anatomopathologique des dépôts amyloïdes dans les tissus. Les biopsies seront guidées par la clinique, en procédant à la méthode la moins invasive. Les biopsies doivent être profondes et intéresser la sous-muqueuse. Les biopsies rectales profondes ont une très bonne rentabilité diagnostique, de 80 à 90%. En revanche, si les biopsies sont superficielles, elles seront, le plus souvent, négatives, les dépôts amyloïdes dans l’ATTRv se retrouvant dans la sous-muqueuse. Les biopsies duodénales, gastriques et œsophagiennes ont également une très bonne rentabilité diagnostique à condition qu’elles intéressent la sous-muqueuse.
Au microscope optique, après coloration au Rouge Congo, on observe un aspect biréfringent en milieu polarisé, très spécifique de la substance amyloïde. Il faut ensuite réaliser un typage afin de préciser le type d’amylose. (2) Si le diagnostic d’amylose est fortement suspecté et que les biopsies digestives ne mettent pas en évidence de dépôts amyloïdes, le diagnostic peut être fait grâce à la biopsie des glandes salivaires accessoires ou par une aspiration de la graisse sous-cutanée abdominale.
Adressage
|
Pour une consultation spécialisée en Gastroentérologie à l’HEGP, contactez Dr Sherine KHATER : sherine.khater@aphp.fr En cas d’adressage pour la réalisation d’une biopsie, faire mention systématique de la « Recherche d’Amylose » sur la demande.
|
(1) Nakov R, Suhrb O.B, Ianiroc G et al. Recommendations for the diagnosis and management of transthyretin amyloidosis with gastrointestinal manifestations. Eur J Gastroenterol Hepatol. 2021 May 1;33(5):613-622
(2) Wixner J, Mundayat R, Karayal ON, Anan I, Karling P, Suhr OB, THAOS investigators. THAOS: gastrointestinal manifestations of transthyretin amyloidosis – common complications of a rare disease. Orphanet J Rare Dis. 2014 Apr 27; 9():61.
PARTIE 6 : CARDIOLOGIE
Rédigée par les Pr. Albert HAGEGE et Dr. Tania PUSCAS
Parmi les amyloses responsables d’une maladie cardiaque, les amyloses AL et les amyloses TTR, sauvages ou wild-type (ATTRwt) et héréditaires/mutées (ATTRh/ATTRm) représentent plus de 98 % des cas d’amylose cardiaque. (1)
Prévalence de l’atteinte cardiaque dans les amyloses et Pronostic au diagnostic
Adapté de Garcia-Pavia P, et al. Eur J Heart Fail. 2021.
| Amylose | Atteinte cardiaque | Médiane de survie au diagnostic | Scores pronostic |
| AL | 70% |
24 mois sans atteinte cardiaque 6 mois si IC au diagnostic et non traité |
Voir : Annexe Scores pronostics |
| ATTRwt | 100% | 57 mois | |
| ATTRm | 30-100% selon la mutation |
31 mois (Val122IIe) 69 mois (autres mutations) |
〉Etape 1 : Suspicion clinique d’Amylose Cardiaque (1)
Contexte clinique cardiaque
- Insuffisance cardiaque (IC) du sujet ≥ 65 ans
- Sténose aortique du sujet ≥ 65 ans
- Hypotension ou normo-tension chez un sujet précédemment hypertendu
- Taux élevés de NT-proBNP et de Troponine T
Les signes extracardiaques
- Surdité
- Syndrome du canal carpien bilatéral
- Rupture du tendon du biceps
- Sténose lombaire
- Purpura périorbitaire
- Macroglossie
- Insuffisance rénale
- Protéinurie
- Polyneuropathie
- Dysautonomie
- Dépôts vitréens
- Histoire familiale
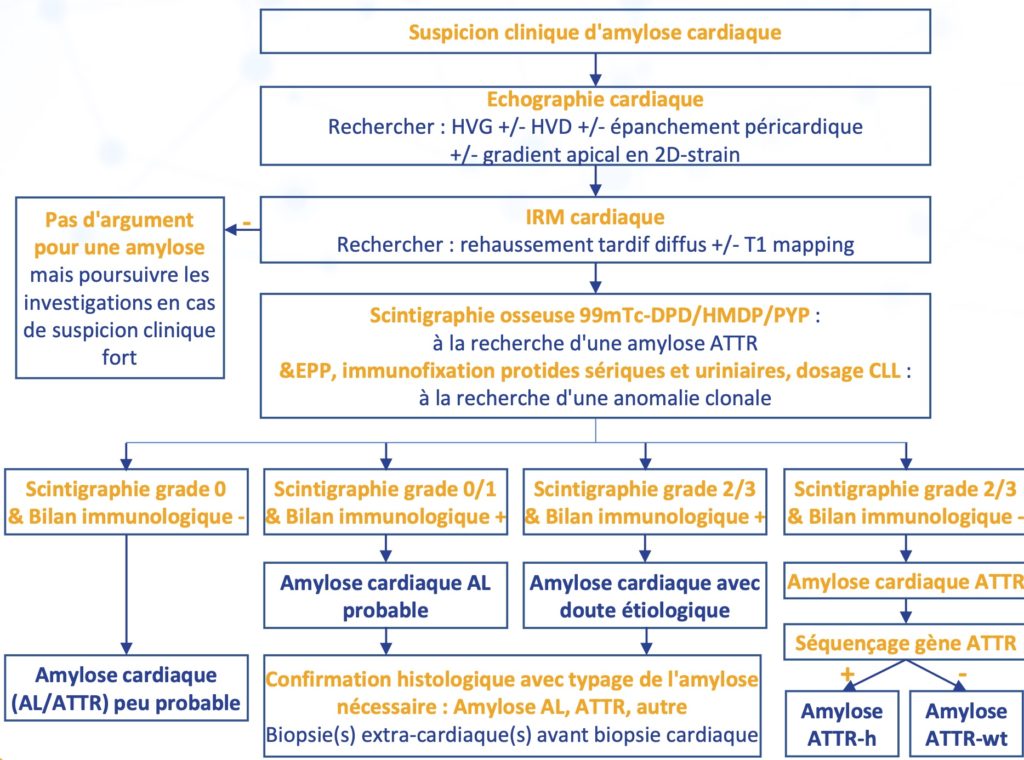
Algorithme diagnostic de l’Amylose Cardiaque
D’après Bodez D, et al. Presse Med. 2016.
〉Etape 2 : Electrocardiogramme (3)
- Micro-voltage QRS ou voltage paraissant insuffisant en regard du degré d’HVG échographique
- Troubles de la conduction auriculo-ventriculaire
- Troubles du rythme à l’étage atrial ou ventriculaire
〉Etape 3 : Echocardiographie (3,4)
- Hypertrophie concentrique du ventricule gauche (HVG) ou biventriculaire
- Augmentation de l’épaisseur des valves atrioventriculaires, du septum inter atrial
- Aspect brillant et granité du myocarde
- Dilatation et dysfonction de l’oreillette gauche
- Dysfonction diastolique avec flux transmitral restrictif
- Réduction du strain global longitudinal avec préservation du strain apical
Voir : Fiche CARDIO – Adressage des patients pour consultation Cardiologique à la recherche d’Amylose
〉Etape 4 : IRM (4)
- Augmentation du volume extra-cellulaire (VEC)
- Augmentation du T1 mapping
- Rehaussement tardif du gadolinium (RTG) avec impossibilité d’annuler le signal myocardique
Voir : Fiche RADIOLOGIE – Adressage des patients en Radiologie pour IRM cardiaque
|
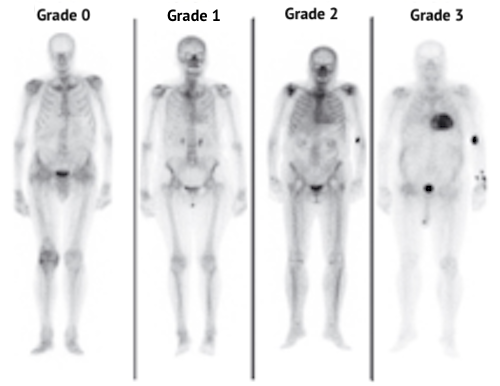
〉Etape 5 : Scintigraphie (1) Fixation cardiaque selon le score de Perugini Voir : Fiche MED NUCL. – Adressage des patients en Médecine nucléaire pour Scintigraphie osseuse |
 |
〉Etape 6 : Biologie (1)
- Electrophorèse des protéines sériques à la recherche d’une gammapathie
- Immunofixation des protéines sériques urinaires (Protéinurie de Bence-Jones 24h)
- Dosage pondéral des immunoglobulines sériques et des chaînes légères libres
Voir : Partie 3 Hématologie
〉Etape 7 : Histologie (5)
| Site de prélèvement | AL | ATTRm | ATTRwt |
| Graisse abdominale | 79-84% | 45-67% | 14-15% |
| Peau | 100% | 94% | 63-73% |
| Glandes salivaires accessoires | 81-89% | 91-100% | – |
| Estomac / Duodenum | 72-95% | 86-100% | 38% |
| Endomyocardique (6) | – | 100% | 100% |
〉Etape 8 : Génétique
La conduite d’une consultation génétique et la réalisation d’un séquençage à la recherche d’une mutation de la transthyrétine est préconisée systématiquement chez tout patient diagnostiqué d’une ATTR, sans critère d’âge.
Voir : Fiche GENETIQUE – Consultation génétique et Séquençage pour l’Amylose
(1) Garcia-Pavia P, et al. Diagnosis and treatment of cardiac amyloidosis. A position statement of the European Society of Cardiology Working Group on Myocardial and Pericardial Diseases. Eur J Heart Fail. 2021 Apr;23(4):512-526.
(2) Bodez D, et al. Les amyloses cardiaques : les reconnaître et les prendre en charge [Cardiac amyloidosis: How to recognize them and manage them?]. Presse Med. 2016 Oct;45(10):845-855. French.
(3) Maurer MS, et al. Addressing Common Questions Encountered in the Diagnosis and Management of Cardiac Amyloidosis. Circulation. 2017 Apr 4;135(14):1357-1377.
(4) Witteles RM, et al. Screening for Transthyretin Amyloid Cardiomyopathy in Everyday Practice. JACC Heart Fail. 2019 Aug;7(8):709-716.
(5) Kitaoka H, et al. Japanese Circulation Society Joint Working Group. JCS 2020 Guideline on Diagnosis and Treatment of Cardiac Amyloidosis. Circ J. 2020 Aug 25;84(9):1610-1671.
(6) Fine NM, et al. Yield of noncardiac biopsy for the diagnosis of transthyretin cardiac amyloidosis. Am J Cardiol. 2014 May 15;113(10):1723-7.
PARTIE 7 : RYTHMOLOGIE
Rédigée par le Dr Pierre BAUDINAUD
L’atteinte cardiaque de l’amylose est souvent compliquée de troubles conductifs et d’arythmies supra ventriculaires et ventriculaires.
Ces troubles sont liés à la présence de dépôts amyloïdes au sein du myocarde, de leur caractère cytotoxique mais également à la dénervation cardiaque liée à l’atteinte neurologique de l’amylose.
La prévalence de ces atteintes et leurs caractéristiques dépend du type d’amylose et de la durée d’évolution de la pathologie.
Il n’est pas rare qu’ils surviennent avant que l’atteinte cardiaque de l’amylose ne soit identifiée.
- Dans une série américaine récente (1), 10 % des patients suivis étaient porteurs d’un stimulateur cardiaque pour un bloc atrio-ventriculaire de haut grade avant que le diagnostic d’amylose ne soit posé. Dans cette même série, la moitié des patients présentaient sur l’ECG de référence un bloc de branche complet.
- Concernant les troubles du rythme, la fibrillation atriale est l’arythmie la plus souvent retrouvée dans cette pathologie avec selon les séries 10 à 69 % (2) des patients atteints.
Dans le cadre du bilan des troubles conductifs et d’arythmies chez le sujet jeune sans cause évidente retrouvée, il faut réaliser un bilan morphologique et biologique complet comprenant entre-autre une recherche d’atteinte cardiaque de l’amylose.
Pour adresser vos patients à l’unité de Rythmologie de l’HEGP afin de réaliser une évaluation, contactez Dr Pierre BAUDINAUD :
|
Secrétariat : 01.56.09.57.37. |
